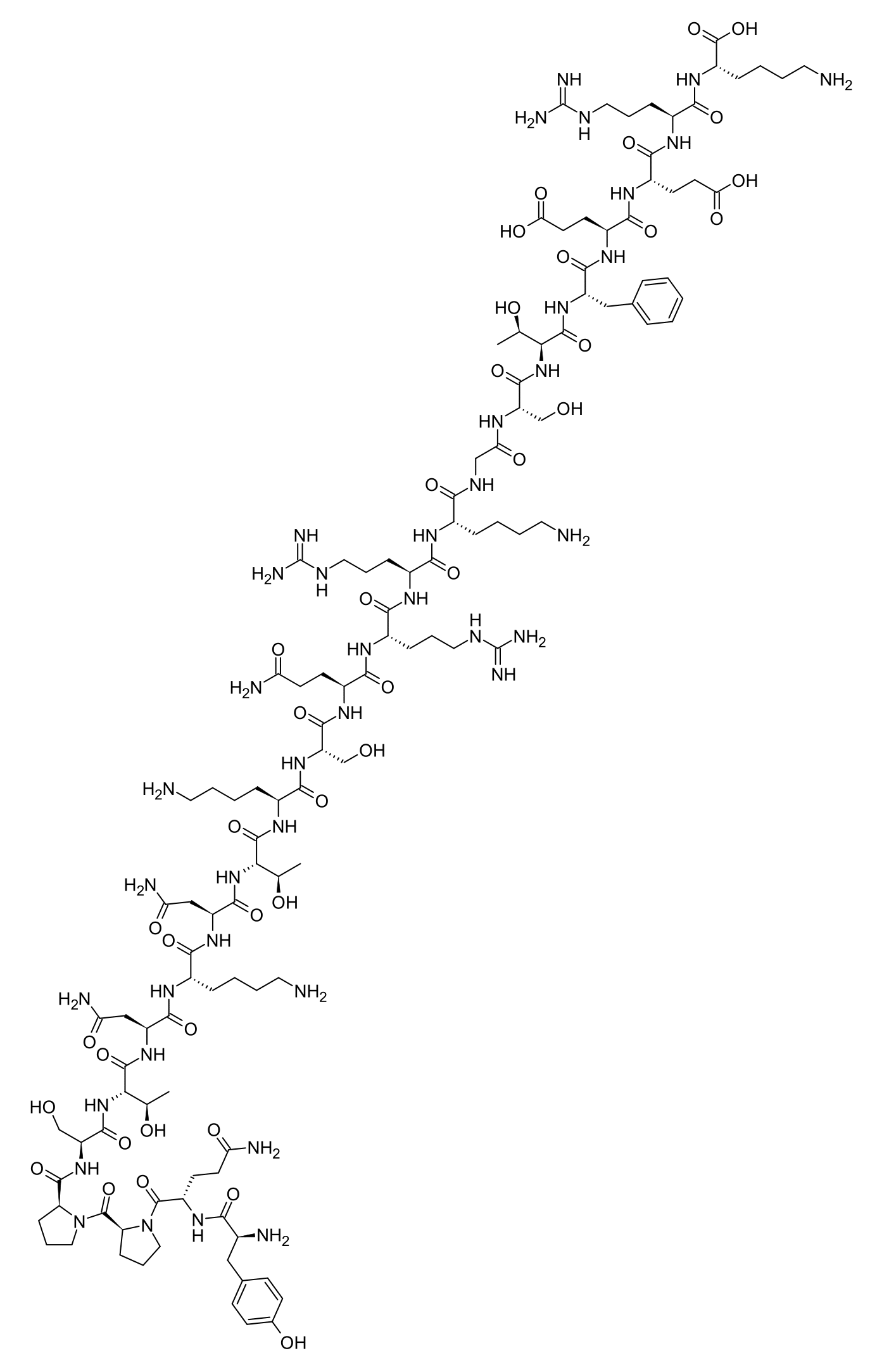
Studien berichten, dass das MGF-E-Peptid (das aktive Prinzip von PEG-MGF) ein durch mechanische Belastung induziertes 24-Aminosäure-Peptid ist, das in präklinischen Studien Myoblasten-Proliferation, Satellitenzell-Aktivierung und Muskelregeneration fördert. Der Rezeptor des MGF-E-Peptids ist 2026 NICHT eindeutig identifiziert; mehrere Studien berichten IGF-1R-UNABHÄNGIGE Aktivität (Mills 2007 PMID 17442731), während andere Studien IGF-1R-abhängige Effekte berichten (Brisson & Barton 2012 PMID 22802461) — der Mechanismus ist eine OFFENE Frage. Die PEGylierung soll die sehr kurze native Plasma-Halbwertszeit (~5–7 min; Hill & Goldspink 2003 PMID 12605581) verlängern; eine peer-reviewte humane PK-Charakterisierung von PEG-MGF existiert NICHT. Beobachtet in Forschungssettings; ausschließlich für Forschungszwecke.
Die Biochemie von PEG-MGF wird von zwei Schlüsselpunkten dominiert. ERSTENS — die Identität des Wirkstoffs: das aktive Prinzip ist das 24-Aminosäure-MGF-E-Peptid (Sequenz YQPPSTNKNTKSQRRKGSTFEERK), das C-terminale E-Domänen-Peptid der IGF-1Ec-Spleißvariante des humanen IGF-1 (UniProt P05019 Isoform 4 / Ec). Mechanische Belastung der Skelettmuskulatur (Stretch, Krafttraining) erhöht schnell die Expression des IGF-1Ec-Spleißisoforms auf Kosten des systemischen IGF-1Ea-Isoforms (Goldspink 1999 PMC1467788; Yang & Goldspink 2002 PMID 12270704); nach posttranslationaler Prozessierung der IGF-1Ec-Prä-Prä-Hormone trennen sich die reife 70-aa-IGF-1-Kette und das 24-aa-MGF-E-Peptid und wirken als ANDERE Moleküle. Das ist der editorische Hauptpunkt der Seite: MGF ist NICHT IGF-1, MGF ist NICHT eine „Variante" oder „Verkürzung" oder „Verlängerung" von IGF-1, sondern ein ANDERES Peptid, das vom selben Gen über alternatives Splicing und Prozessierung erzeugt wird. ZWEITENS — die offene Mechanismus-Frage: studien berichten IGF-1R-UNABHÄNGIGE Aktivität für das MGF-E-Peptid (Mills 2007 PMID 17442731 — das synthetische E-Peptid bindet den IGF-1-Rezeptor NICHT, und mehrere Goldspink-Linien-Mechanismus-Behauptungen wurden NICHT reproduziert), während andere Studien IGF-1R-abhängige Effekte berichten (Brisson & Barton 2012 PMID 22802461). Der definitive Rezeptor des MGF-E-Peptids ist somit als 2026 NICHT eindeutig identifiziert. Dies ist eine OFFENE mechanistische Frage; die Seite muss Phrasen wie „studien berichten" und „der Rezeptor des MGF-E-Peptids ist nicht eindeutig identifiziert" verwenden und niemals implizieren, dass MGF den IGF-1-Rezeptor als etablierten Fakt aktiviert. Die PEGylierung adressiert die sehr kurze native Plasma-Halbwertszeit von ~5–7 Minuten (Hill & Goldspink 2003 PMID 12605581); Vendoren bevorzugen typischerweise 5-kDa- oder 20-kDa-(verzweigtes)-PEG, das N-terminal an den Tyr¹-Rest konjugiert wird. Vendoren behaupten, dass PEG-MGF im Menschen „mehrere Tage" zirkuliert; jedoch wurde KEINE peer-reviewte humane PK-Studie von PEG-MGF veröffentlicht — die exakte humane Halbwertszeit ist nicht charakterisiert. Anti-PEG-Antikörper sind ein dokumentiertes Immunogenitäts-Phänomen für PEGylierte Arzneimittel (z. B. Pegloticase, Peginesatide), das für PEG-MGF spezifisch nicht untersucht wurde — bei chronischer / wiederholter Dosierung ein theoretisches Sicherheits-Bedenken. Beobachtet in Forschungssettings; ausschließlich für Forschungszwecke.