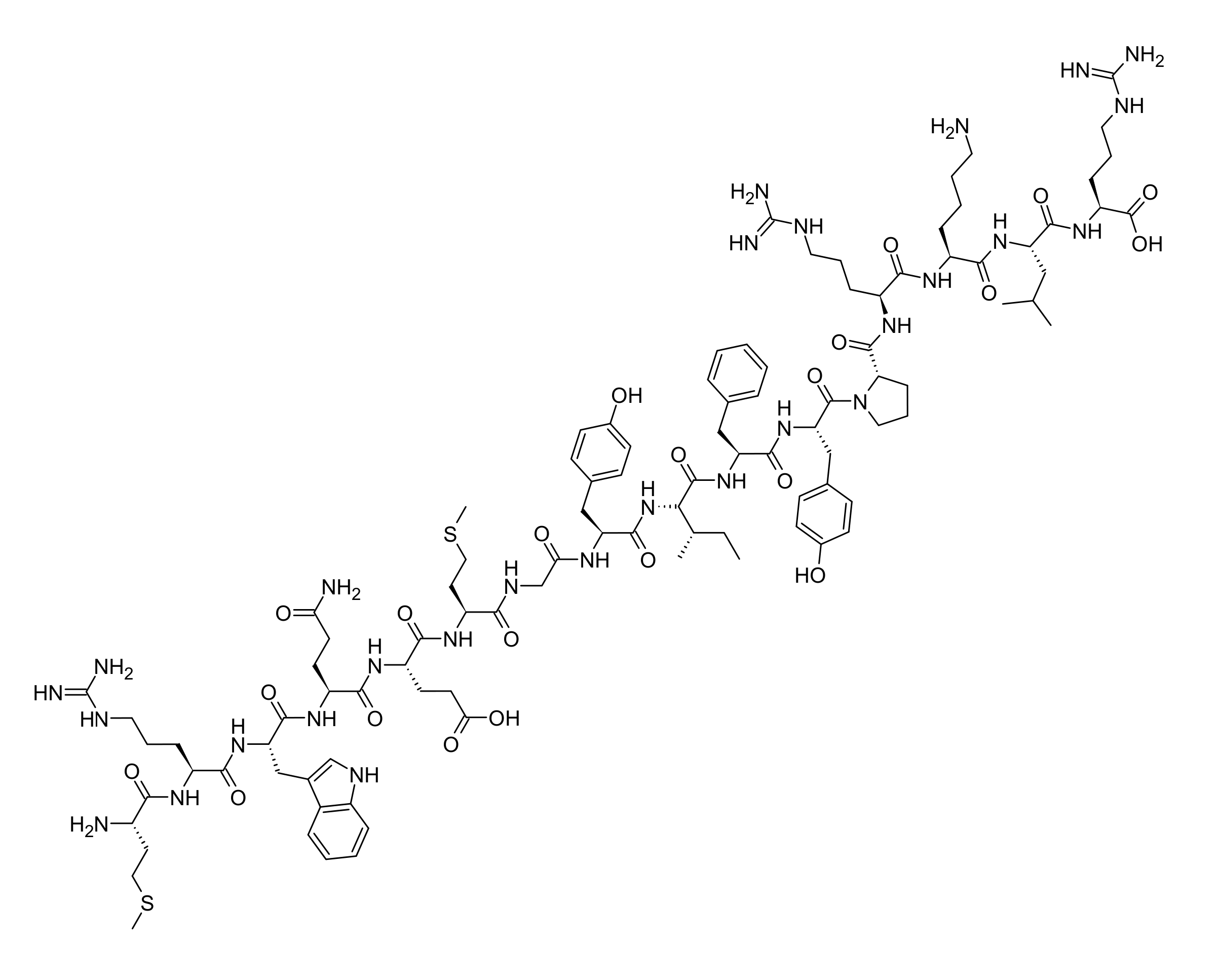
Studien berichten, dass MOTS-c über die Hemmung des Folat-/Methionin-Zyklus intrazelluläres AICAR erhöht und dadurch die AMP-aktivierte Proteinkinase (AMPK) allosterisch aktiviert — primär im Skelettmuskel. Sekundär wird unter metabolischem oder oxidativem Stress eine Translokation aus dem Cytoplasma in den Zellkern beschrieben, wo MOTS-c stress-responsive Transkription moduliert. MOTS-c gilt als retrograder Mitochondrium-zu-Kern-Bioregulator, der zelluläre Bioenergetik mit ganzkörperlicher Glukose-Homöostase koordiniert. Beobachtet in Forschungssettings; ausschließlich für Forschungszwecke.
MOTS-c war das erste Mitglied der MDP-Klasse, dem eine definierte systemische Stoffwechselrolle zugeschrieben wurde. Seine Entdeckung etablierte, dass mtDNA bioaktive Peptide über kleine ORFs innerhalb der rRNA-Gene kodiert — MOTS-c auf MT-RNR1 (12S rRNA) und Humanin sowie SHLP1–6 auf MT-RNR2 (16S rRNA) (Kim/Yen 2021, GeroScience, PMID 32910336). In der initialen Arbeit von Lee et al. 2015 (Cell Metab, PMID 25738459) verhinderte intraperitoneale MOTS-c-Gabe in Mäusen alters- und Hochfett-Diät-induzierte Insulinresistenz und Diät-induzierte Adipositas, mit verbesserter Glukosetoleranz und reduzierter Fettmasse — mechanistisch verortet in einer Skelettmuskel-AMPK-Aktivierung über Hemmung des Folat-/Methionin-Zyklus. Studien berichten, dass MOTS-c unter metabolischem oder oxidativem Stress aus dem Cytoplasma in den Zellkern transloziert, wo es chromatin-assoziierte Faktoren bindet und transkriptionelle Programme in Richtung antioxidativer Abwehr und Stoffwechseladaptation verschiebt (Kim 2018, PMID 29983246). Im Skelettmuskel wirkt MOTS-c als Sport-Mimetikum — endogene Expression steigt nach körperlicher Aktivität und exogene Gabe verbessert metabolische Flexibilität und Laufleistung in Maus-Modellen (Reynolds 2021, PMID 33473109). Wichtige editorielle Eingrenzung: Aussagen zur menschlichen Pharmakologie beruhen überwiegend auf Beobachtungsstudien zu endogenem MOTS-c (Plasma-Spiegel nach Sport, Allel-Varianten); humane Expositionsdaten zu **synthetischem** MOTS-c als Forschungspeptid existieren nicht in peer-reviewter Form, und die einzige in vivo humane Phase-1-Datenbasis stammt von **CB4211**, einem stabilisierten Analog (NCT03998514) und nicht vom natürlichen 16-aa-Peptid. Mechanismus-Aussagen werden daher bewusst hedged formuliert — Studien berichten, beobachtet in Forschungssettings — und niemals als etablierte humane Pharmakologie. Ausschließlich für Forschungszwecke.