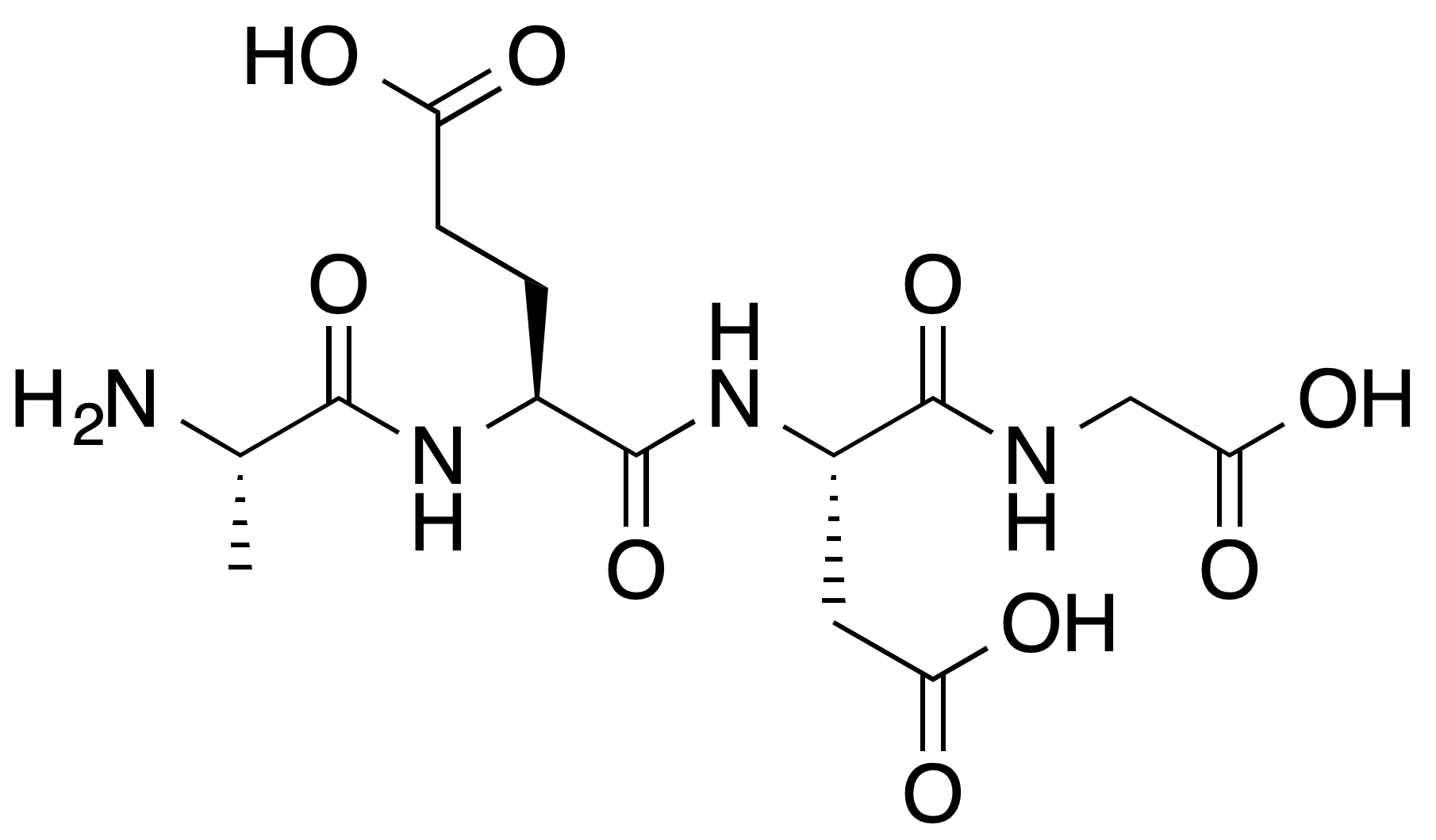
Epitalon (AEDG) wird hypothetisch als Peptid-Bioregulator beschrieben, der Telomerase (TERT) in somatischen Zellen in vitro aktiviert und die pineale Melatonin-Sekretion modulieren soll; sekundär werden epigenetische Effekte über direkte Bindung an die Linker-Histone H1/3 und H1/6 mit selektiver Genexpressions-Aktivierung vorgeschlagen. Ein systemischer Telomerase-Effekt am Menschen in vivo ist nicht peer-reviewed nachgewiesen.
Die mechanistische Literatur zu Epitalon ist überwiegend aus In-vitro-Fibroblasten-Experimenten und Nagetierstudien abgeleitet und nicht durch klinisch belastbare Pharmakokinetik- oder Target-Engagement-Daten am Menschen validiert. Studien berichten in der seminalen Khavinson-2003-Arbeit (Bull Exp Biol Med, PMID 12937682), dass Epithalon, direkt zu telomerase-negativen humanen fetalen Fibroblastenkulturen gegeben, die Re-Expression der katalytischen TERT-Untereinheit, Telomerase-Aktivität und kontinuierliche Zellteilung über den Hayflick-Limit hinaus (Passage 44+ vs. Kontrollstopp bei Passage 34) induzierte — ein In-vitro-Befund, KEIN Beleg für humane In-vivo-Telomerase-Reaktivierung. Die 2025 unabhängige In-vitro-Studie aus Brunel University London und Royal Brompton bestätigte eine dosisabhängige Telomer-Verlängerung in normalen Fibroblasten und Epithelzellen über hTERT-Hochregulation, beobachtete jedoch in Brustkrebs-Zelllinien Verlängerung über den ALT-Pfad — die erste klar nicht-Khavinson-affilierte Replikation des zentralen Telomer-Befundes mit gleichzeitiger Sicherheitsflagge (Al-Dulaimi 2025, PMID 40908429). Die Polnische Übersichtsarbeit von Araj et al. 2025 (Int J Mol Sci, PMID 40141333) hält explizit fest, dass es „ungewiss bleibt, ob dies die einzigen Wirkmechanismen sind" und dass „Informationen zu kritischen Sicherheitsfragen dieses Peptids fehlen". Es existiert keine peer-reviewed humane Pharmakodynamik-Studie, die eine systemische Telomerase-Aktivierung in vivo nach peripherer Epitalon-Gabe nachweist. Mechanismus-Aussagen werden daher bewusst hedged formuliert — Studien berichten, vorgeschlagene Pfade, in vitro beobachtet — und niemals als etablierte humane Pharmakologie. „Anti-Aging"-Marketing, das Epitalon als humanen Telomerase-Aktivator bewirbt, überschreibt das, was die publizierte Evidenz tatsächlich zeigt.