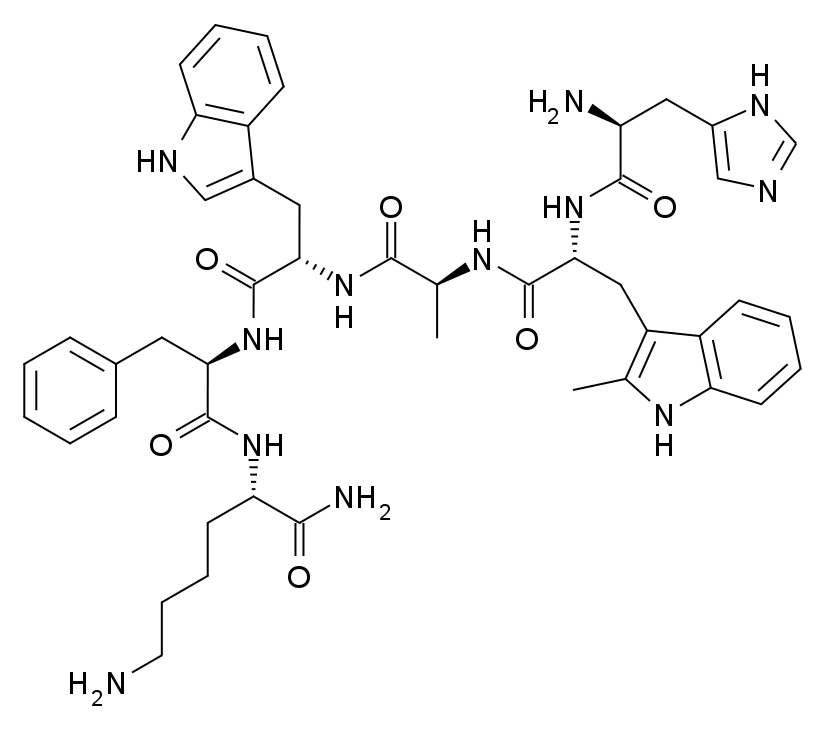
Hexarelin wurde in einer foundational pharmacology paper (Deghenghi 1994), Phase-I-PK/PD-Arbeiten zu Bioverfügbarkeit und Hormonprofil (Imbimbo 1994; Ghigo 1994; Massoud 1996), einer longitudinalen pädiatrischen Pharmakologie-Studie (Klinger 1996), drei humanen kardiovaskulären Studien (Bisi 1999; Imazio 2002; Broglio 2002), der kanonischen CD36-Mechanismus-Arbeit (Bodart 2002), einem zeitgenössischen Review (Mao 2014) und einer präklinischen post-MI-Studie (McDonald 2018) untersucht. Befunde werden als investigativ und ausschließlich für Forschungszwecke berichtet.
Akute GH-Freisetzungspharmakologie bei gesunden Erwachsenen — multiple Verabreichungswege (Ghigo 1994)
Phase I Studien berichten in einer Open-Label-PK/PD-Studie an N=12 gesunden jungen männlichen Probanden, dass die GH-Freisetzung nach 1 µg·kg⁻¹ i.v. Hexarelin etwa doppelt so groß war wie nach 1 µg·kg⁻¹ GHRH. Bioverfügbarkeit: subkutan 77,0 ± 10,5 %, intranasal 4,8 ± 0,9 %, oral 0,3 ± 0,1 %; Plasma-Halbwertszeit ≈ 55 Minuten.
— Ghigo et al., J Clin Endocrinol Metab 1994;78(3):693–698 (PMID 8126144)
Dosis-Wirkungs-Beziehung von GH, Prolaktin und Cortisol (Massoud 1996)
Phase I Studien berichten in einer Dosis-Wirkungs-Studie an gesunden männlichen Erwachsenen (Hexarelin 0–1,0 µg·kg⁻¹ i.v.) eine maximale GH-Freisetzung mit Plateau bei ~140 mU·L⁻¹ (ED₅₀ ≈ 0,48 µg·kg⁻¹), einen Prolaktin-Anstieg um bis zu 180 % über Baseline (ED₅₀ ≈ 0,39 µg·kg⁻¹) und einen Cortisol-Anstieg um ~40 % bei 0,5 µg·kg⁻¹ — quantitativ deutlich mehr als bei Ipamorelin. Die Kombination aus niedrigdosiertem Hexarelin (0,125 µg·kg⁻¹) plus GHRH erzeugte massive GH-Freisetzung (~115 mU·L⁻¹) bei minimaler Cortisol-Erhöhung.
— Massoud et al., J Clin Endocrinol Metab 1996;81(12):4338–4341 (PMID 8954038)
Akuter inotroper Effekt am Herzen gesunder Menschen (Bisi 1999)
Phase I Studien berichten in einer Cross-over-hormonell/kardiovaskulären Studie an N=7 gesunden männlichen Probanden mittels Radionuklid-Angiokardiographie eine LVEF-Erhöhung von 64,0 ± 1,5 % auf 70,7 ± 3,0 % (P < 0,03) nach i.v. Hexarelin, mit Maximum bei 30 Minuten und ~60-minütiger Persistenz, OHNE signifikante Veränderung von mittlerem Blutdruck oder Herzfrequenz. Rekombinantes humanes GH (rhGH) erzeugte trotz vergleichbarem GH-Anstieg KEINEN inotropen Effekt — konsistent mit einer GH-unabhängigen myokardialen Wirkung (später CD36 zugeschrieben).
— Bisi et al., J Endocrinol Invest 1999;22(4):266–272 (PMID 10342360)
CD36 als molekularer kardialer Rezeptor — Knockout-Pharmakologie (Bodart 2002)
preclinical Studien berichten in einem Rezeptor-Identifikations-Experiment in isolierten Rattenherzen, dass Hexarelin in Wildtyp-Herzen einen dosisabhängigen Anstieg des koronaren Perfusionsdrucks erzeugte, während diese Antwort in CD36-defizienten Herzen TROTZ erhaltener GHSR-1a-Expression vollständig aufgehoben war. Damit wurde CD36 als der kardiale Rezeptor für Hexarelin und andere GHRPs etabliert.
— Bodart et al., Circ Res 2002;90(8):844–849 (PMID 11988484)
Kardiale Funktion bei Patienten mit koronarer Herzkrankheit (Broglio 2002)
Phase II Studien berichten in einer offenen intra-operativen Studie während Bypass-Chirurgie an N=24 männlichen KHK-Patienten (mittleres Alter 59,5 J.) einen prompten Anstieg von LVEF, Cardiac Index und Cardiac Output (alle P < 0,001) innerhalb von 10 Minuten nach i.v. Hexarelin, mit Persistenz bis zu 90 Minuten und OHNE Veränderungen des linksventrikulären enddiastolischen Volumens oder des systemischen Gefäßwiderstands. Weder rhGH noch GHRH reproduzierten diese hämodynamischen Verbesserungen — konsistent mit einem nicht-GH-vermittelten kardialen Mechanismus.
— Broglio et al., Eur J Pharmacol 2002;448(2-3):193–200 (PMID 12144941)
Kardiotrope Aktivität bei linksventrikulärer Dysfunktion (Imazio 2002)
Phase II Studien berichten in einer offenen kardiotropen Vergleichsstudie an N=13 Patienten (8 dilatative + 5 ischämische Kardiomyopathie) bei i.v. Einzeldosis-Hexarelin, dass die LVEF bei ischämischer, NICHT aber bei dilatativer Kardiomyopathie anstieg — trotz vergleichbarem hexarelin-induziertem GH-Anstieg in beiden Gruppen. Der inotrope Effekt erfordert offenbar vitales Myokard, das auf direkte CD36/GHSR-vermittelte kardiotrope Signalwege ansprechen kann.
— Imazio et al., Eur J Heart Fail 2002;4(2):185–191 (PMID 11959048)
GHSR-1a-Desensitisierung bei Langzeitdosierung (Klinger 1996)
observational Studien berichten in einer offenen longitudinalen Pharmakologie-Studie an N=7 prä-pubertären kleinwüchsigen Kindern (mittleres Alter 7,6 J.) bei intranasalem Hexarelin 60 µg·kg⁻¹ dreimal täglich über 6–10 Monate, dass der GH-Peak von 70,6 mU·L⁻¹ Baseline auf 34,1 mU·L⁻¹ nach 7 Tagen fiel (~50 % Abnahme) und dann plateau erreichte — Bestätigung einer Rezeptor-Desensitisierung. Trotz biochemischer Toleranz stieg die Wachstumsgeschwindigkeit von 5,3 ± 0,9 cm·Jahr⁻¹ vor Behandlung auf 7,4 ± 1,6 cm·Jahr⁻¹ nach 6–10 Monaten. Folgestudien zeigen ~50–75 % AUC-GH-Abnahme über 4–16 Wochen täglicher Dosierung, partiell reversibel nach Auswaschperiode — Wellness-Markt-Behauptungen einer dauerhaften „anti-aging"-Erhöhung sind durch diese Evidenz NICHT gestützt.
— Klinger et al., Eur J Endocrinol 1996;134(6):716–719 (PMID 8766941)