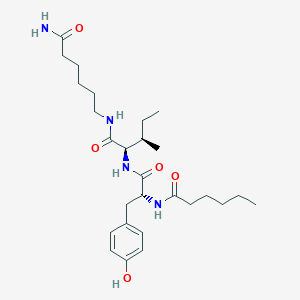
Studien aus der Harding-Gruppe an der Washington State University berichten, dass Dihexa als positiver Modulator des Hepatozyten-Wachstumsfaktor (HGF) / c-Met-Rezeptor-Systems funktioniert und HGF-getriebenes MAPK- und PI3K-AKT-Signalling sowie dendritische Spinogenese, hippokampale LTP und Synaptogenese augmentiert. Dihexa ist KEIN Angiotensin-II-Rezeptor-Agonist (weder AT1 noch AT2) trotz seiner Angiotensin-IV-Linie. Beobachtet in Forschungssettings.
Die mechanistische Erzählung der WSU-Gruppe lautet: Angiotensin-IV-abgeleitete Peptide wirken nicht über klassische Angiotensin-Rezeptoren, sondern über das zerebrale HGF/c-Met-Neurotrophsystem. Dihexa, das metabolisch stabilisierte und gehirngängige Angiotensin-IV-Analogon, soll laut McCoy 2013 und Benoist 2014 die HGF-Bindung an c-Met potentieren, durch Dimerisierungs-Disruption die HGF-Aktivität bei niedrigen Konzentrationen paradox AUGMENTIEREN und die Dichte dendritischer Dornfortsätze in hippokampalen Kulturen erhöhen. In Verhaltensstudien wurde berichtet, dass Dihexa scopolamin-induzierte Morris-Wasser-Labyrinth-Defizite in Ratten umkehrt, die Performance gealterter Ratten verbessert und (Sun 2021) die kognitive Leistung sowie die Neuroinflammation in APP/PS1-transgenen Alzheimer-Modellmäusen rettet. Die häufig zitierte Aussage „Dihexa ist sieben Größenordnungen (≈ 10 Millionen-fach) potenter als BDNF" stammt SPEZIFISCH aus Benoist 2014 — einer Arbeit, die am 29. April 2025 vom Journal of Pharmacology and Experimental Therapeutics formal ZURÜCKGEZOGEN wurde. Triscience behandelt diese Potenz-Behauptung als unverifiziert mit Audit-Datum 2026-05-02 und empfiehlt Auslassung aus Marketing-artigen Texten. Die breitere HGF/c-Met-als-kognitives-Ziel-Hypothese bleibt ein aktives Forschungsgebiet und wurde von Athira Pharma mit dem separaten Molekül Fosgonimeton (ATH-1017 / NDX-1017) in klinische Studien übersetzt — Fosgonimeton scheiterte jedoch 2023 an seiner Phase-2/3-LIFT-AD-Studie, was die Pfad-Validierungs-Erzählung weiter schwächt. Mechanismus-Aussagen werden hier bewusst hedged formuliert — Studien berichten, beobachtet in Forschungssettings — und niemals als etablierte humane Pharmakologie. Ausschließlich für Forschungszwecke.