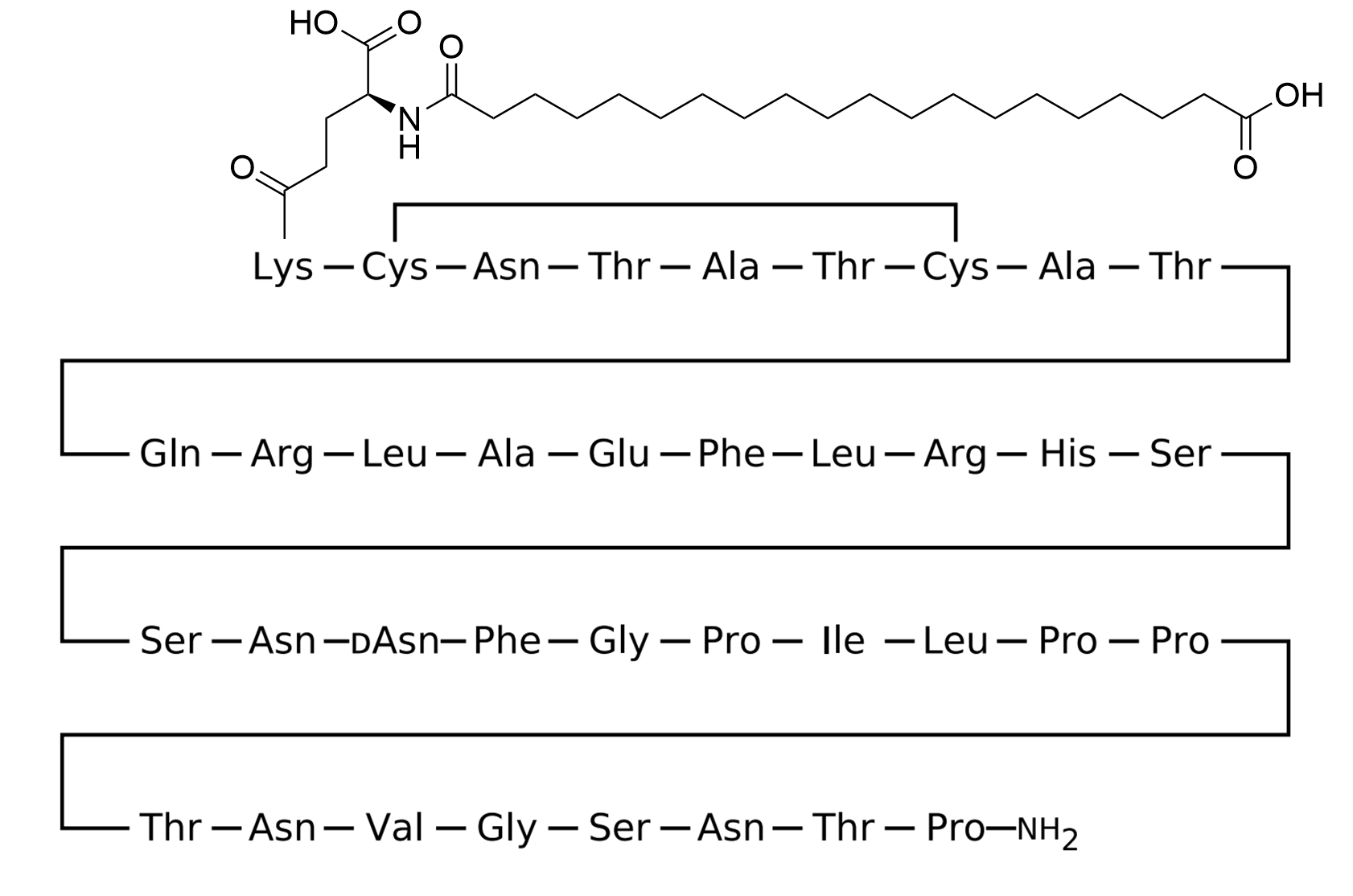
CagriSema kombiniert dualen Amylin/Calcitonin-Rezeptoragonismus (durch Cagrilintid) mit GLP-1-Rezeptoragonismus (durch Semaglutid) und wirkt damit auf zwei komplementäre zentrale und periphere Sättigungspfade gleichzeitig.
Die pharmakologische Begründung der Kombination beruht auf der Beobachtung, dass GLP-1- und Amylin-Rezeptor-Agonismus auf teilweise unterschiedliche Schaltkreise im Hirnstamm und im Hypothalamus wirken, die sich aber in der Appetit-Suppression und Reduktion der Energieaufnahme treffen. Die Phase-2-Studie von Frías et al. (Lancet 2023) zeigte bei T2D-Patienten unter CagriSema eine Gewichtsabnahme von −15,6 % gegenüber −5,1 % unter Semaglutid allein und −8,1 % unter Cagrilintid allein nach 32 Wochen. In der Phase-3-Studie REDEFINE 1 (Garvey et al., NEJM 2025) lag die mittlere Gewichtsabnahme nach 68 Wochen bei −20,4 % (CagriSema) gegenüber −14,9 % (Semaglutid 2,4 mg), −11,5 % (Cagrilintid 2,4 mg) und −3,0 % (Placebo). Diese Daten quantifizieren den additiven Nutzen des dualen Pfad-Engagements bei Adipositas ohne Diabetes. Die strukturbiologische Aufklärung der Cagrilintid-Bindung an Calcitonin- und Amylin-Rezeptoren wurde 2025 von Cao et al. (Nat Commun 2025) publiziert. Der Beitrag jedes Bestandteils zur Halbwertszeit von ca. 7 Tagen beruht auf der nicht-kovalenten Albuminbindung über die C20-Diacid-Acylierung (Cagrilintid) bzw. die C18-Diacid-Acylierung (Semaglutid).