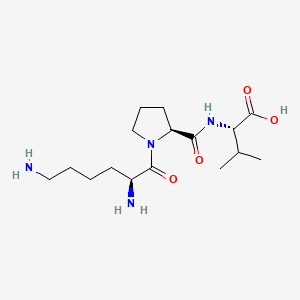
Die publizierte Evidenzbasis ist überwiegend präklinisch (Maus in vivo + in-vitro-Zellkultur und Antimikrobiell-Assays). Die Hiltz / Catania / Lipton-Linie von 1989–1991 etablierte das α-MSH(11–13)-Pharmakophor-Konzept; die Dalmasso 2008 / Kannengiesser 2008-IBD-Arbeiten lieferten die murinen Kolitis-Wirksamkeitsdaten und die PepT1-Mechanismus-Beschreibung. Die Brzoska 2008 Endocr-Rev-Übersichtsarbeit bietet die rezeptor-unabhängige Synthese. ClinicalTrials.gov-v2-API-Audit am 2. Mai 2026: NULL aktive registrierte humane Studien für KPV-als-Tripeptid (siehe REGISTRY-LÜCKE oben). Beobachtet in Forschungssettings.
DSS-induzierte Kolitis (Maus) — in vivo, IBD-Wirksamkeit
in vivo Studien berichten, dass orale KPV-Gabe Körpergewichtsverlust, histologische Entzündung und pro-inflammatorische Zytokin-Expression (IL-6, TNF-α, IL-1β) gegenüber Vehikel-Kontrollen reduzierte. Mechanistisch verbunden mit SLC15A1 / PepT1-vermittelter apikaler Aufnahme in entzündetes Kolon-Epithel.
— Dalmasso et al. 2008, Gastroenterology 134(1):166-178 (PMID 18061177)
TNBS-induzierte Kolitis (Maus) — in vivo, IBD-Wirksamkeit
in vivo Studien berichten, dass orale KPV-Gabe Disease Activity Index (DAI) und histologische Entzündung gegenüber Vehikel-Kontrollen reduzierte. Konsistent mit dem PepT1-vermittelten Liefermodell.
— Dalmasso et al. 2008, Gastroenterology 134(1):166-178 (PMID 18061177)
CD45RBhi-T-Zell-Transfer-Kolitis (Maus) — in vivo, rezeptor-unabhängiger Test
in vivo Studien berichten, dass KPV die Gewichtswiedererlangung und histologische Scores verbesserte; der Effekt blieb in MC1R-defizienten Mäusen teilweise erhalten und unterstützt die rezeptor-unabhängige antiinflammatorische Aktivität.
— Kannengiesser et al. 2008, Inflamm Bowel Dis 14(3):324-331 (PMID 18092346)
PepT1-vermittelte zelluläre Aufnahme — in vitro, Caco-2 / HT29-Zellkulturen
in vitro Studien berichten, dass KPV ein Substrat des Protonen-gekoppelten Di-/Tripeptid-Transporters SLC15A1 / PepT1 ist (Kₘ ≈ 160 μmol/L) und nanomolar NF-κB- und MAP-Kinase-Signalling in intestinalen Epithelzellen und Immunzellen hemmt.
— Dalmasso et al. 2008, Gastroenterology 134(1):166-178 (PMID 18061177)
Antimikrobielle Aktivität — in vitro, Staphylococcus aureus und Candida albicans
in vitro Studien berichten, dass α-MSH und das C-terminale Tripeptid KPV S. aureus-Koloniebildung hemmten und C. albicans-Vitalität und Keimrohrbildung reduzierten. Vorgeschlagener Mechanismus: Erhöhung des mikrobiellen cAMP; der Adenylyl-Cyclase-Inhibitor ddAdo hob die Tötungsaktivität teilweise auf. HINWEIS: Konzentrationen sind höher als der nanomolare antiinflammatorische Bereich; keine klinische antimikrobielle Anwendung etabliert.
— Cutuli et al. 2000, J Leukoc Biol 67(2):233-239 (PMID 10670585)
Humane Keratinocyten-Signalling — in vitro, Calcium-vermittelte Antworten
in vitro Studien berichten, dass KPV calcium-vermittelte Antworten in humanen Keratinozyten ohne Erhöhung des cAMP auslöst — DISTINKT vom klassischen MC1R-cAMP-Pfad, der durch Volllängen-α-MSH aktiviert wird. Unterstützt die rezeptor-unabhängige Mechanismus-Erzählung.
— Elliott et al. 2004, J Invest Dermatol 122(4):1010-1019 (PMID 15102092)
Anti-inflammatorische Pharmakophor-Charakterisierung — in vivo, frühe Mausmodelle
in vivo Studien berichten, dass die α-MSH(11–13)-Sequenz und stereochemische Analoga (D-Lys, D-Pro, D-Val-Substitutionen) antiinflammatorische / antipyretische Aktivität in Mausmodellen erhalten — was etablierte, dass die antiinflammatorische Pharmakophor-Region von α-MSH innerhalb der C-terminalen drei Reste lokalisiert ist. Die Hiltz / Catania / Lipton-Arbeiten bilden die foundational-zitate für die KPV-Forschungslinie.
— Hiltz et al. 1991, Peptides 12(4):767-771 (PMID 1788140)
Synthese des rezeptor-unabhängigen Modells — Übersichtsarbeit
preclinical Übersichtsarbeit synthetisiert die Hypothese, dass α-MSH-C-terminale Tripeptide (KPV, ähnliche Analoga) antiinflammatorische Wirkungen WEITGEHEND OHNE klassische Melanocortin-Rezeptor-Agonismus ausüben — eine Schlüssel-Disambiguierung gegenüber MC1R-Pigmentierungs-Agonisten (Afamelanotid, Melanotan II) und MC4R-Sexual-Funktions-Agonisten (PT-141 / Bremelanotid).
— Brzoska et al. 2008, Endocrine Reviews 29(5):581-602 (PMID 18612139, Übersichtsarbeit)